Definizione
I leiomiomi uterini, anche definiti miomi o fibromi, sono neoplasie benigne a partenza dalle cellule muscolari lisce che compongono il miometrio, cioè il muscolo uterino. Possono avere diametro compreso tra pochi millimetri e diversi centimetri. Sono il più delle volte asintomatici essendo un reperto diagnostico occasionale all’esame ultrasonografico; nel restante dei casi, invece, sono riscontrati per sintomi quali dolori mestruali (dismenorrea), mestruazioni abbondanti (menorragia), dolore pelvico, infertilità o aborti ricorrenti, fino ai casi in cui le dimensioni della formazione miomatosa sono tali da determinano la comparsa di fenomeni compressivi a carico degli organi pelvici (necessità di urinare spesso per compressione della vescica o difficoltà a defecare per compressione del retto.
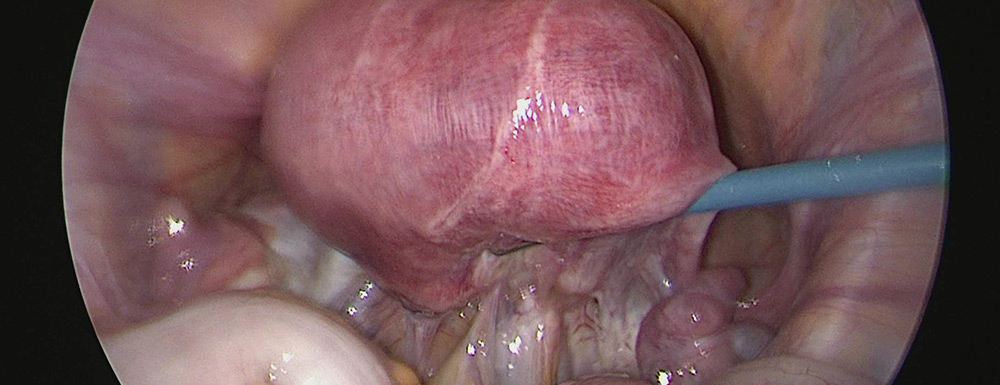
La localizzazione dei miomi ne determina il tipo, la sintomatologia e il trattamento. Possono svilupparsi interamente nello spessore del miometrio (intramurali o interstiziali – 70%), protrudere nella cavità peritoneale attraverso la sierosa uterina (sottosierosi – 20%, sessili o peduncolati) o possono aggettarsi all’interno della cavità uterina (sottomucosi – 10%, sessili o peduncolati). Poiché spesso non è possibile definire una precisa delimitazione delle formazioni fibrose, si ricorre a descrizioni intermedie tra quelle sopra indicate (es: intramurale-sottomucoso etc…). Evenienza meno frequente è la sede cervicale dei miomi (fig 1).

Le localizzazioni intramurali o sottomucose sono più spesso correlate a disordini di tipo mestruale, come menorragia (30-40%), determinando frequentemente anemizzazione e alterazioni della qualità di vita della paziente; i miomi sottosierosi, invece, risultano per lo più asintomatici, fatta eccezione per i rari casi di sintomi da compressione esercitata dalle grosse dimensioni del fibroma. Il dolore è un sintomo poco frequente ed è spesso associato alla torsione del peduncolo o alla dilatazione cervicale determinata dai miomi sottomucosi in espulsione.
Fisiopatologia
Il ruolo degli ormoni ovarici
Numerosi studi in vitro hanno dimostrato il ruolo cardine degli ormoni prodotti dall’ovaio nella genesi dei miomi, che infatti sono riscontrati tipicamente in età fertile, aumentano di volume in gravidanza e regrediscono dopo la menopausa. Gli ormoni sessuali agiscono attraverso un meccanismo in parte mediato dai fattori di crescita locali. Rispetto al normale miometrio, i leiomiomi presentano inoltre un’abnorme espressione di recettori per estrogeni e progesterone, che determina un’elevata sensibilità a tali ormoni durante la fase proliferativa del ciclo mestruale.
Diverse evidenze suggeriscono che i fibromi uterini sono influenzati da fattori genetici. È stato per esempio dimostrato che gemelle monozigoti hanno il doppio del tasso di concordanza per isterectomia rispetto alle gemelle dizigoti. Il ruolo genetico è rilevante anche nella familiarità esistente nella comparsa dei fibromi, con un rischio di miomatosi uterina da 2 a 6 volte superiore nelle donne che abbiamo una parente di primo grado affetta da tale patologia. Infine, esistono specifiche sindromi genetiche in cui, associate ad altre lesioni specifiche, vi sono i leiomiomi uterini.
Sintomatologia
Come già affermato, in una buona percentuale dei casi i leiomiomi sono del tutto asintomatici e sono diagnosticati in occasione di controlli ginecologici praticati di routine. Il sintomo più frequente della miomatosi uterina è la menorragia, cioè la mestruazione di entità aumentata, talvolta associata a sanguinamento irregolare e prolungato, fino a quadri più severi che comportano anemizzazione della paziente. I fibromi possono essere causa di infertilità specie se si sviluppano in corrispondenza degli osti tubarici o occupano la cavità uterina ostacolando l’impianto della camera gestazionale. In corso di gravidanza possono, invece, rendersi responsabili di aborti o parti pretermine, nonché di eventi emorragici del post-partum e del puerperio.
Il dolore è sintomo caratteristico dei leiomiomi intracavitari, per le contrazioni esercitate dall’utero nel tentativo di espellere la formazione. In questi casi, se il mioma è peduncolato, il peduncolo tenderà ad allungarsi e il mioma può arrivare a dilatare la cervice uterina. Il dolore è invece più caratteristico dei miomi intramurali. Più frequentemente il dolore è sostituito da una sensazione gravativa in regione pelvica. I già citati fenomeni compressivi determinano invece una sintomatologia differente a seconda dell’area interessata.
Diagnosi
L’esame ginecologico bimanuale fornisce spesso le prime indicazioni circa la presenza di un fibroma uterino. Nella valutazione di queste formazioni possono essere utili diversi esami, fra cui l’ecografia transvaginale e/o trans addominale, l’isteroscopia, e la risonanza magnetica (MRI). L’ecografia transvaginale grazie alla sua natura non-invasiva ed al basso costo rappresenta l’esame iniziale consigliato. L’esame MRI è preferito quando occorre una mappatura precisa del mioma (solitamente per scopi chirurgici), ma rappresenta l’esame associato al costo economico più elevato. L’isteroscopia consente non solo di confermare la presenza e l’estensione di un mioma sottomucoso, ma anche di praticare biopsie su aree con aspetti iperplastici. L’isterosalpingografia è invece consigliabile quando alla presenza di un mioma si associa una condizione di sterilità.
Strategie terapeutiche
La scelta del trattamento da attuare in pazienti con fibromatosi uterina dovrebbe tener conto di alcuni punti chiave: il rapporto rischio-beneficio delle diverse modalità terapeutiche; il tasso di recidiva e, quindi, la necessità di terapie ripetute o aggiuntive; l’impatto di un trattamento ripetuto; il desiderio di prole della paziente; la sintomatologia; il volume e la sede dei fibromi; l’effetto della terapia sulla qualità di vita della paziente.
Chirurgia
L’approccio chirurgico alla fibromatosi deve essere considerato soprattutto nei quadri di sanguinamenti severi e anemia e quando ogni tentativo di intervento medico, quando possibile, non ha dato alcun miglioramento significativo della situazione clinica della paziente. Le modalità di approccio chirurgico sono molteplici: miomectomia laparotomica o laparoscopica, asportazione di miomi per via isteroscopica, ablazione endometriale e, come opzione radicale, l’isterectomia laparotomica, laparoscopica o vaginale. Esistono pochi studi in letteratura che mettano a confronto le varie opzioni terapeutiche disponibili (mediche e chirurgiche), in termini di risultati a lungo termine e di miglioramento dei sintomi soggettivi delle pazienti. L’intervento chirurgico appare il trattamento di prima scelta per le pazienti con menorragia, dolore o senso di peso pelvico, urgenza minzionale e incontinenza urinaria, ossia in tutte quelle situazioni in cui la presenza di miomi sintomatici influisce sulla qualità della vita della donna.
La miomectomia, che consiste unicamente nell’asportazione dei noduli fibrosi, è indicata nelle pazienti con miomi sintomatici che desiderano preservare la capacità procreativa L’intervento può essere eseguito per via laparotomica, laparoscopica o isteroscopica, se la sede è sottomucosa. La miomectomia laparotomica ha rappresentato l’approccio chirurgico conservativo, alternativo all’isterectomia, maggiormente utilizzato negli anni, essendo in grado di ridurre i sintomi nell’80% delle pazienti ma soprattutto perché non presenta maggiore morbilità perioperatoria rispetto all’intervento demolitivo (49,50,51). Essa si associa ad un tasso di gravidanze a termine post chirurgiche che oscilla tra il 50-60 %.
Alcuni studi hanno dimostrato che il verificarsi della rottura uterina in caso di gravidanza dopo miomectomia è un evento raro pari al 0,5-1% e può essere correlato alla tecnica chirurgica. La miomectomia laparoscopica consiste nell’accesso minimamente invasivo, alternativo alla miomectomia laparotomica, nei fibromi intramurali e sottosierosi, quando il numero dei fibromi da rimuovere è uguale o inferiore a 3-5 e il diametro è inferiore a 9 cm (58).
Numerosi studi prospettici randomizzati hanno confrontato la miomectomia laparoscopica con la tecnica a cielo aperto, dimostrando che la prima è associata ad un minore dolore post-operatorio, minore perdita di sangue, a minor tempo di degenza e a minori accessi ospedalieri. Inoltre, con l’approccio laparoscopico, vi è una minore incidenza e severità della comparsa di aderenze postoperatorie, che possono incidere negativamente sulla fertilità, causare dolore pelvico cronico, incrementare il rischio di gravidanza ectopica e di rottura di utero gravido e, occasionalmente, provocare occlusione intestinale.
La miomectomia per via isteroscopica rappresenta un altro approccio chirurgico efficace esclusivamente nel trattamento dei fibromi sottomucosi che rappresentano la causa del 5-10% dei sanguinamenti uterini anomali, dolore, sub-fertilità ed infertilità. Il successo della procedura dipende dal tipo di mioma, dalle dimensioni dell’utero, dal numero dei fibromi e varia dal 65% al 100%. Dopo miomectomia isteroscopica i tassi di fertilità appaiono eccellenti e non ci sono state segnalazioni di casi di rottura uterina.
Di recente, grazie ai progressi raggiunti nell’ambito della chirurgia laparoscopica, la miomectomia può essere eseguita usando la chirurgia robotica. Questo nuovo approccio rappresenta una valida alternativa agli accessi tradizionali. Tuttavia, tale procedura presenta ancora dei limiti soprattutto in termini economici e di training chirurgico che non ne permette l’applicazione su larga scala.
Le pazienti con fibromatosi uterina diffusa e sintomatica, resistente alla terapia medica e non desiderose di prole, sono invece candidate all’intervento di isterectomia. Tra le complicanze associate all’isterectomia va menzionato il rischio di abbondanti perdite ematiche intra-operatorie e tempi di degenza ospedaliera più lunghi. L’isterectomia può essere praticata per via vaginale, per via addominale oppure per via vaginale assistita laparoscopicamente.
Va ricordato che l’approccio vaginale non può essere praticato in tutte le pazienti, in quanto esso richiede delle dimensioni uterine inferiori a quelle di un utero gravido a 16 settimane di gestazione. In pazienti selezionate, quindi, l’approccio vaginale presenta numerosi vantaggi rispetto all’isterectomia vaginale assistita laparoscopicamente, tra cui la minore durata dell’intervento, la minore esposizione ai farmaci anestesiologici ed i ridotti costi complessivi (73). Ad ogni modo, i risultati ottenuti con le due tecniche sono pressoché sovrapponibili.
Paragonando l’approccio laparoscopico a quello tradizionale, l’isterectomia per via addominale, si hanno numerosi vantaggi derivanti da una tecnica meno invasiva, tra i quali: minore sanguinamento intra-operatorio, minore dolore post-operatorio e, quindi, tempi di ricovero più brevi. Tutto ciò senza un aumento dei rischi intra-operatori, ma, addirittura, in alcuni casi, garantendo una minore incidenza di complicanze post-operatorie.
Embolizzazione delle arterie uterine
In casi opportunamente selezionati un’alternativa al trattamento chirurgico dei miomi è rappresentata da una tecnica di radiologia interventistica: l’embolizzazione delle arterie uterine (UAE), il cui razionale si basa sulla possibilità di effettuare l’embolizzazione delle rete arteriosa perilesionale assicurando al tempo stesso una perfusione normale del miometrio sano..
I dati della letteratura mostrano un elevato tasso di successo della embolizzazione dei fibromi uterini, soprattutto quando si effettua l’accesso bilaterale, con riduzione del volume e miglioramento della sintomatologia nel 75-85% dei casi. Durante i primi sei mesi la riduzione volumetrica del mioma è massima ed evidente, essa continua nei mesi successivi anche se in maniera più modesta, fino a riscontrare una riduzione del volume del 30-46%.
La maggior parte delle pazienti sviluppa, dopo due ore dalla procedura, perdite vaginali ed importante sintomatologia dolorosa tale da richiedere trattamento farmacologico per il controllo del dolore (cosiddetta “sindrome da postembolizzazione”)..
Un aspetto importante da sottolineare è l’aumentato rischio di anomalie di impianto placentare dopo UAE: circa il 13% delle donne sottoposte a tale procedura, nullipare e senza altri fattori di rischio, ha avuto una forma di placenta previa o accreta.
Ultrasuoni focalizzati
L’ablazione con ultrasuoni focalizzati guidati dalla risonanza magnetica (MR guided Focused Ultrasound o MRgFUS) è una procedura non invasiva che sfrutta gli ultrasuoni per distruggere le alterazioni benigne dell’utero come i fibromi uterini e le adenomiosi, senza alterare i tessuti sani circostanti. La terapia con ultrasuoni focalizzati utilizza l’energia delle onde acustiche (ultrasuoni) per eliminare le cellule del fibroma uterino in modo del tutto non-invasivo, senza quindi incidere la cute. L’energia degli ultrasuoni viene focalizzata in un punto specifico dove determina un aumento della temperatura (superiore a 70°C) fino a distruggere le cellule, solo nel punto in cui si sta trattando. Questa terapia si ottiene utilizzando le immagini della Risonanza Magnetica come una guida in tempo reale ma anche come controllo dell’effetto terapeutico. Durante la procedura la paziente è cosciente, solo parzialmente sedata e interagisce con l’operatore. Il risultato finale è una necrosi del tessuto fibromatoso che sarà riassorbito dal corpo in un tempo variabile a seconda del soggetto. La terapia con ultrasuoni focalizzati ha come effetto immediato quello di ridurre la sintomatologia sia legata al sanguinamento (in seguito alla necrosi cellulare) che alla sensazione di peso (rendendo più morbido il fibroma) (90). L’efficacia della procedura è variabile nelle varie casistiche ma mediamente è riportata una riduzione dei sintomi del 50% circa a dodici mesi. La letteratura riporta un’incidenza di successiva isterectomia fra il 5 e il 10%.
Le complicanze sono molto rare e la più comune è rappresentata dalle ustioni cutanee (1-7% dei casi). Complicanze meno frequenti sebbene di maggiore entità sono rappresentate da: metrorragia profusa, dolore e sanguinamento vaginale persistente, nausea, paralisi del nervo sciatico e, seppur descritto in un solo caso, perforazione intestinale e vescicale.
Nelle pazienti che hanno concepito dopo la procedura si è osservata in una serie di 51 pazienti, esito positivo della gravidanza nel 41% dei casi. Gli effetti sulla struttura e sull’integrità del miometrio sono purtroppo ancora indefiniti e per questo motivo attualmente questo trattamento è sconsigliato alle donne desiderose di future gravidanze.
Terapie farmacologiche
La terapia medica è attuabile nelle pazienti che, per la presenza di miomi o fibromatosi uterina, presentano una sintomatologia molesta o ingravescente e nelle pazienti desiderose di prole. Inoltre, la terapia medica trova indicazione, in attesa dell’intervento chirurgico per ridurre le dimensioni dei noduli o dell’utero che andranno asportati o per migliorare un’eventuale condizione di anemia.
Agonisti del GnRH (GnRH-a)
Questi farmaci sopprimo la produzione di FSH (e di LH) da parte dell’ipofisi e, conseguentemente bloccano la produzione di estradiolo da parte dell’ovaio. Lo stato “similmenopausale” che ne consegue conduce a riduzione di volume dell’utero e dei fibromi che, in alcuni trial, ha raggiunto il 50-70%.
La loro assunzione va protratta al massimo per 3-6 mesi. Dopo trattamento con GnRH-a, l’intervento chirurgico risulta più agevole e breve, con minore perdita ematica, minore ricorso ad incisioni laparotomiche longitudinali, possibilità di un approccio vaginale o conservativo in un maggior numero di pazienti e decorso post-operatorio più breve. Tuttavia, il costo elevato, gli importanti effetti collaterali simil-menopausali (vampate di calore, atrofia vaginale, accelerata perdita della massa ossea, ecc.) e l’efficacia transitoria (effetto “rebound” alla sospensione del trattamento) rendono il loro impiego limitato alla fase preoperatoria. Le attuali linee guida internazionali suggeriscono che l’uso di GnRH-agonisti è utile prima dell’intervento, ma affermano anche che per ogni individuo il beneficio deve essere valutato rispetto al costo e gli effetti collaterali.
Per migliorare i sintomi menopausali connessi all’uso di questi composti, essi vengono talora associati ad altri farmaci:
- GnRH analoghi + estro-progestinici (add back therapy);
- GnRH analoghi + tibolone;
- GnRH analoghi + Raloxifene.
Modulatori selettivi del recettore del progesterone (SPRMs)
I due principali prodotti proposti per la terapia dei fibromi appartenenti a questa categoria sono ulipristal acetato (UPA) ed il mifepristone o RU486, ma solo l’UPA è in commercio con questa indicazione. L’efficacia e la sicurezza dell’UPA nel management dei fibromi uterini sono state dimostrate attraverso una serie di 4 trials clinici. Questi studi hanno dimostrato che, in donne con sintomatologia severa conseguente a fibromi uterini, la somministrazione di UPA è significativamente superiore al placebo nel ridurre rapidamente l’entità del sanguinamento ed il volume dei fibromi; è superiore ad un analogo del GnRH nel mantenere la riduzione del volume dei fibromi dopo la sospensione della terapia; non si associa a sintomi e complicanze da ipoestrogenismo ed è quindi proponibile sia come trattamento preoperatorio a breve termine sia come trattamento prolungato per il controllo cronico della sintomatologia.